
Добро пожаловать в наш блог, посвященный увлекательному миру германия и других фотоэлектрических материалов.

Прогресс в исследованиях по изготовлению генератора Ge-Германия-68
Недавно исследователи нашего научно-исследовательского центра самостоятельно разработали процесс разделения и очистки Ge-германия-68.

Лучшее время для покупки Ge-германия? Последняя динамика рынка
Цены на внутреннем рынке германия продолжают расти, а поставщики по-прежнему неохотно идут на продажи.
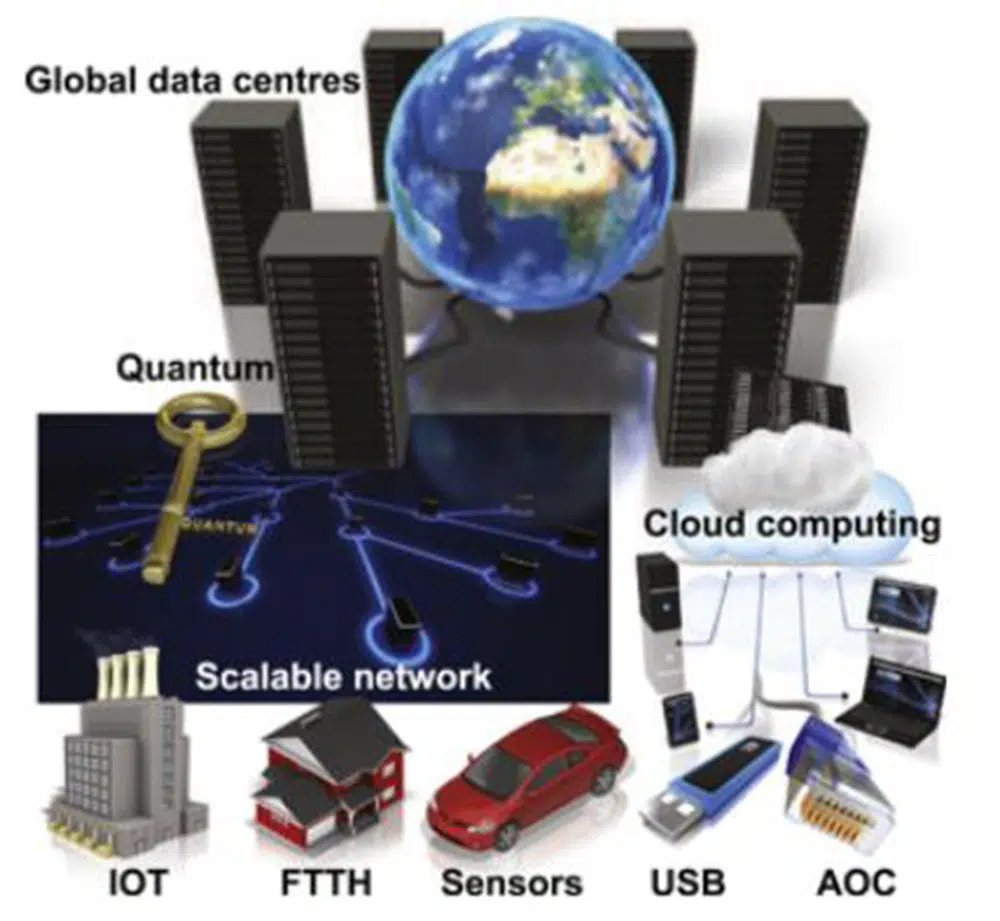
Инновационные применения источника света на основе германия
Интернет вещей обещает произвести революцию в способах общения с использованием глобальной сети датчиков, при этом потребности в коммуникациях в центрах обработки данных будут расти экспоненциально.







